4. Diagnostik
Ausführliche Richtlinien zur mikrobiologischen Diagnostik der Lyme-Borreliose wurden von der Deutschen Gesellschaft für Hygiene und Mikrobiologie (DGHM) publiziert.
Untersuchungsmaterial
Geignete Materialien für die mikrobiologische Diagnostik sind in einer Übersicht dargestellt.
| Klinische Manifestation | Untersuchungsmaterial | |
|---|---|---|
| Erregernachweis | Antikörpernachweis | |
| Stadium I (früh / lokalisiert) - Tage bis Wochen nach Zeckenstich | ||
| Erythema migrans | Hautbiopsie | Serum |
| Stadium II (früh / disseminiert) - Wochen bis Monate nach Zeckenstich | ||
| Multiple Erytheme | Hautbiopsie | Serum |
| Borrelien Lymphozytom | Hautbiopsie | Serum |
| Karditits | (Myocardbiopsie) | Serum |
| Neuroborreliose | Liquor | Liquor/Serum Paar |
| Ophthalmoborrliose | Serum | |
| Stadium III (spät / persisten) | ||
| Arthritis | Gelenk Punktat, Synovia Biopsie | Serum |
| Acrodermatitis chronica atrophicans | Hautbiopsie | Serum |
| Chronisch progrediente Enzephalomyelitis | Liquor | Liquor/Serum Paar |
In der Praxis wird oft serologischen Verfahren wegen der einfacheren Durchführung der Vorzug gegeben, jedoch sollte vor allem bei diagnostisch schwierigen Fällen sowie von wertvollem Biopsiematerial der Erregernachweis angestrebt werden. Geeignetes Material für den Erregernachweis sind verschiedene Körperflüssigkeiten (Liquor cerebrospinalis, Gelenkpunktat) sowie Biopsiematerial (Haut, Synovialis, in besonderen Fällen auch Herz- und Hirnbiopsien). Der Antikörpernachweis erfolgt normalerweise aus Serum. Bei V.a. Neuroborreliose sollte grundsätzlich auch Liquor cerebrospinalis (Liquor/Serum-Paar vom selben Tag erforderlich) untersucht werden. Gelenkpunktat ergibt beim Antikörpernachweis nahezu identische Antikörpertiter, daher ist eine zusätzliche serologische Untersuchung von Gelenkpunktat (auch aus Kostengründen) nicht sinnvoll.
Erregernachweis
Der direkte mikroskopische Nachweis ist für Patientenproben ungeeignet. Für Patientenproben müssen empfindlichere Verfahren, wie der kulturelle Nachweis oder die Polymerase-Kettenreaktion (PCR) durchgeführt werden. Die Wahrscheinlichkeit eines positiven Erregernachweises ist in erheblichem Maße vom Untersuchungsmaterial abhängig, wobei hier PCR und Kultur etwa gleichwertig sind für Haut- und Liquorproben, mit Ausnahme der höheren Empfindlichkeit der PCR bei Gelenkpunktaten.
Erfolgsrate beim Erregernachweis
Patientenproben (Kultur, PCR)
| Untersuchungsmaterial | Erfolgsrate |
|---|---|
| Haut (Erythema migrans, ACA) | 50 - 70 % mit Kultur oder PCR |
| Liquor (Neuroborreliose II) | 10 - 20 % mit Kultur oder PCR |
| Gelenkpunktat (Lymearthritis)* | 50 - 70 % mit PCR (Kultur extrem selten positiv) |
* höhere Sensivität des Erregernachweises aus Synovialis Biopsie
Zecken (Immunfloureszenz, Kultur, PCR)
Erfolgsrate: Abhängig von Entwicklungsstadium der Zecke und Endemiegebiet
Kultureller Erregernachweis
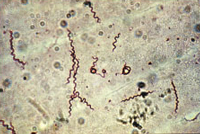
Kulturpräparat: Fuchsinfärbung
- Beimpfen von Spezial-Medium (MKP) mit der Probe (Haut, Liquor, etc.)
- wöchentliche Wachsumskontrollen: Farbumschlag des Mediums (rosa/gelb), Dunkelfeldmikroskopie
- wöchentliche Subkulturen bis 6 Wochen
Die PCR aus Urin und Blut kann nach dem derzeitigen Wissensstand nicht für die Diagnostik empfohlen werden. Mittels Immunfluoreszenz können Borrelien in der Zecke nachgewiesen werden, z.B. für wissenschaftliche Fragestellungen wie Durchseuchungsraten von Zecken mit Borrelien. Der Erregernachweis in Zecken von Patienten mit dem Ziel daraus therapeutische Konsequenzen zu ziehen, wird nicht empfohlen. Der Erregernachweis mittels PCR und Kultur sollte nur in spezialisierten Laboratorien durchgeführt werden (z.B. im Nationalen Referenzzentrum für Borrelien). Die Indikationen für den Erregernachweis sollten auf besondere Fälle beschränkt werden, wie z.B. Hautmanifestationen mit atypischer Symptomatik nach Zeckenstich (Hautbiopsie), V.a. akute Neuroborreliose bei negativer Serologie, V.a. Lyme-Arthritis (PCR von Gelenkpunktat oder Synovialisbiopsie). Die Befunde sollen bei positiven Erregernachweis die Speziesdiagnose enthalten (Typisierung der Isolate bzw. Sequenzanalyse der PCR-Amplicons).
Polymerase Kettenreaktion (PCR)
Nested PCR, Zielsequenz: ospA Gen
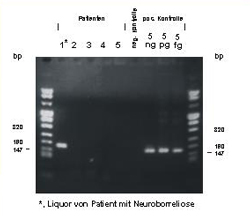
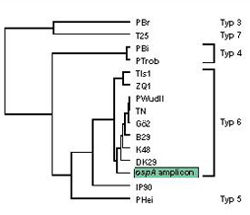
Polymerase Kettenreaktion (PCR): Agarosegel der PCR Produkte (links), Sequenzanalyse des ospA Amplicons (rechts)
Antikörpernachweis

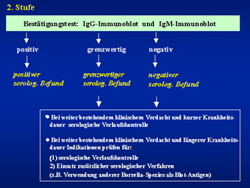
Abbildungen: Stufendiagnostik
Serologische Untersuchungen sollen grundsätzlich als Stufendiagnostik durchgeführt werden. Als 1. Stufe (oben links) wird der ELISA empfohlen, der Immunblot darf erst in der 2. Stufe (oben rechts) eingesetzt werden. Es ist zu empfehlen, ELISAs hoher Sensitivität bei gleichzeitig guter Spezifität (Zweit-Generationsteste) als Suchteste zu verwenden, weil das die Spezifität insgesamt verbessert. Die Standardisierung der serologischen Tests, insbesondere des Immunblot, stellt noch ein großes Problem dar. Die Verwendung rekombinanter Antigene erlaubt eine zuverlässige Identifikation immunreaktiver Borrelienproteine. Bei Verwendung von Ganzzell-Lysaten dagegen ist die Identifikation spezifischer Borrelienproteine sehr viel schwieriger und muss durch Mitführen von monoklonalen Antikörpern und Referenzseren sichergestellt sein.
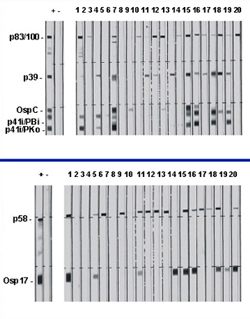
Abbildungen: Rekombinanter igG Immunblot: links oben: Antigene: p83/100, p39, OspC p41i (internes Falgellinfragment); links unten: Antigene: p58 und Osp17;
Standardisierung des Immunblot: rechts: mit Referenzseren (G=IgG, M=IgM) und monoklonalen Antikörpern (MAKs, 1-11); Antigen: B. afzelii (Stamm PKo)
Die für amerikanische Patienten entwickelten Kriterien sind auf die europäische Situation nicht übertragbar, es müssen daher für die europäische Situation entwickelte Kriterien verwendet werden.
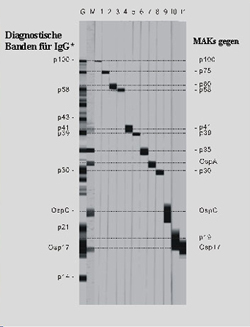
Interpretationskriterien für den IgG Immunblot
Ganz Zell Lysat Immunblot*: positiv, wenn >= 2 Banden der folgenden vorhanden sind: p83/100, p58, p43, p39, p30, OspC, p21, Osp17, p14
Rekombinaner Immunblot: positiv, wenn >= 2 Banden der folgenden vorhanden sind: p83/100, p58, p39, OspC, p41int, Osp17
* Bei Verwendung von Stamm PKo (B. afzelii)
Alle Banden müssen eine Mindest Intensität entsprechend einer schwach positiven Kontrolle aufweisen
Serologische Befunde und Interpretation
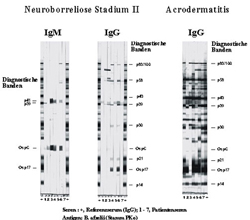
Ganz-Zell-Lysat-Immunblot
Grundsätzlich ist der Antikörpernachweis bei Patienten mit kurzer Krankheitsdauer oder mit lokalisierter Infektion eher negativ. IgM-Antikörper sind in der Regel früher als IgG-Antikörper nachweisbar, jedoch wurden auch Fälle von Erythema migrans und Neuroborreliose ohne IgM-Antikörpernachweis bei positivem IgG-Antikörpernachweis beobachtet.
Im Immunblot findet sich in Regel bei Frühmanifestationen eine Immunantwort gegen wenige Borrelienproteine, bei Spätmanifestationen dagegen eine Immunantwort gegen ein breites Antigenspektrum (serologische Befunde). Bei Spätmanifestationen sind in der Regel IgG-Antikörper nachweisbar, ein negativer IgG-Befund spricht gegen das Vorliegen einer Spätmanifestation. Auf der anderen Seite differenziert ein positiver IgG-Befund (auch hohe Antikörpertiter) nicht zwischen klinisch manifester Infektion und einem Durchseuchungstiter. Der isolierte Nachweis von IgM-Antikörpern bei V.a. chronische Manifestationen der Lyme-Borreliose ist diagnostisch nicht verwertbar; d. h. bei Fehlen von IgG-Antikörpern spricht der alleinige Nachweis von IgM-Antikörpern gegen die Diagnose einer chronischen Lyme-Borreliose. Serologische Verlaufskontrollen werden insbesondere zur Diagnostik der Frühmanifestationen angeraten. Serokonversionen werden auch nach Antibiotika-Therapie noch gesehen, auf der anderen Seite kann eine frühe Antibiotika-Therapie die Bildung von Antikörpern hemmen. Die Eignung der Serologie zur Therapiekontrolle ist allerdings fraglich, die Therapiekontrolle mittels Serologie wird daher nicht empfohlen.
| Stadium | seropositiv | IgM versus IgG |
|---|---|---|
| I | 20 - 50 % | Prävalenz von lgM bei kurzer Krankheitsdauer und |
| II | 70 - 90 % | Prävalenz von IgG bei längerer Krankheitsdauer |
| III | 90 - 100 % | in der Regel nur IgG isolierter IgM Befund spricht gegen LB II |
Liquor/Serum-Index
Einen sehr hohen Stellenwert hat die Bestimmung des erregerspezifischen Liquor/Serum-Index für die Diagnose der Neuroborreliose . Hierzu werden Liquor und Serum vom selben Tag untersucht. Gesamtimmunglobulin wird in beiden Proben gemessen und - nach Einstellung der Proben auf identische Immunglobulinkonzentrationen - die ELISA-Einheiten in Liquor und Serum bestimmt. Ein Faktor > 2,0 spricht für intrathekale Borrelien-spezifische Antikörperproduktion. Der bloße Nachweis von Antikörpern im Liquor ist dagegen nicht aussagekräftig, da im Liquor nachweisbare Antikörper auch aus dem Serum des Patienten stammen können (d. h. passiv übertragen sein können). Vor allem bei kurzer Krankheitsdauer kann die intrathekale Immunantwort bereits vor der Serum-Immunantwort nachweisbar sein. Der erhöhte erregerspezifische Liquor/Serum-Index ist der wichtigste mikrobiologische Parameter für die Diagnose der chronisch progredienten Neuroborreliose und ein wichtiges diagnostisches Kriterium zur Abgrenzung gegen die Multiple Sklerose.
MiQ12 Lyme-Borreliose
Die englische Version der Richtlinien der Deutschen Gesellschaft für Hygiene und Mikrobiologie zur mikrobiologischen Diagnostik der Lyme-Borreliose (MiQ 12, Lyme-Borreliose) stehen im Internet zur Verfügung unter

